Клиническая микробиология
Задача микробиологических исследований в учреждениях здравоохранения - это диагностика возбудителей инфекционных заболеваний и определение чувствительности к антибактериальным препаратам для определения тактики лечения пациентов. Проведение бактериологических исследований крайне важно, ведь именно они позволяют повысить точность постановки диагноза и избежать проблем, связанных с антибиотикорезистентностью. Результаты микробиологических анализов являются основой мониторинга и прогноза эпидемиологической ситуации.
В ходе бактериологических исследований проводят посев собранного у пациента биоматериала на питательную среду, что способствует росту и размножению возбудителя заболевания. При этом выявляется не только факт наличия того или иного заболевания, но и концентрация патогенных микроорганизмов.
Бактериологическое исследование состоит из нескольких этапов:
-
Выделение чистой культуры и получение изолированных колоний
-
Накопление чистой культуры
-
Идентификация чистой культуры
В основе микробиологических исследований лежит культивирование на питательных средах и окраска по Граму, что на сегодняшний день остаётся «золотым стандартом» микробиологического тестирования и позволяет качественно и точно выделить искомого возбудителя, а также определить чувствительность к антибактериальным препаратам.
Приготовление сред в лаборатории
Специалисты бактериологических лабораторий могут варить среды самостоятельно или использовать готовый продукт. Приготовление питательных сред - это сложный и трудоемкий процесс. Он требует от лаборатории самостоятельного подбора компонентов, контроля рецептуры, корректировки рН и соблюдения стерильных условий. Кроме того, учреждение несёт дополнительные затраты на электроэнергию и водоснабжение. При этом срок годности питательных сред, приготовленных в лаборатории, - всего 5-7 дней (у “промышленных” - до 80 суток.
Важно, существует ряд агаров, самостоятельное приготовление которых в лаборатории особенно затруднительно. Речь идёт о кровяных агарах. Добавление человеческой донорской крови в состав среды недопустимо, а используемая кровь животных должна иметь соответствующие сертификаты.
Этапы самостоятельного приготовления сред:
-
Закупка сырья и организация его хранения
-
Приготовление с соблюдением установленной рецептуры
-
Контроль качества
Компания “БиоВитрум” развивает собственное производство готовых питательных сред в чашках Петри под брендом «Средофф» и высококачественных красителей по Граму.
Такие среды как колумбийский агар, агар с бараньими эритроцитами, шоколадный агар с лошадиной кровью производства «Средофф» позволяют провести качественную изоляцию труднокультивируемых микроорганизмов таких как Neisseria, Haemophilus, Streptococcus и других.
Среды, приготовленные в промышленных масштабах, стабильны по своему составу. Каждый продукт производится, согласно протоколу, по отлаженной технологии, со строгим контролем качества на всех этапах производства. Согласно клиническим рекомендациям, готовые к использованию среды не подвергаются внутрилабораторному контролю качества. Всё это существенно экономит время лаборантов.
“БиоВитрум” является дистрибьютором продукции для бактериологических исследований производителя с мировым именем компании Thermo Fisher Scientific. Экспресс-наборы для диагностики от Thermo Fisher Scientific (Oxoid/Remel) позволяют быстро подтвердить наличие и свойства возбудителей.
Антибиотикорезистентность
Одной из глобальных проблем здравоохранения на сегодняшний день является невосприимчивость микроорганизмов (бактерий, вирусов, некоторых паразитов) к воздействию противомикробных препаратов. Как следствие, стандартные методы лечения теряют эффективность, инфекции не поддаются лечению и передаются окружающим. По данным ВОЗ высокие показатели устойчивости к противомикробным препаратам, часто используемым для лечения распространенных инфекций, указывают на то, что в мире становится все меньше эффективных способов борьбы с этими заболеваниями. Например, показатель устойчивости к ципрофлоксацину, противомикробному препарату, часто используемому для лечения инфекций мочевыводящих путей, в 33 представивших данные странах варьируется от 8,4% до 92,9%.
Компания “БиоВитрум” предлагает комплексное решение для определения чувствительности микроорганизмов к антибактериальным препаратам:
-
Готовые питательные среды “Средофф” (агар МХ и агар МХ с ЛК). Соответствуют Клиническим рекомендациям МЗ РФ КР «Определение чувствительности микроорганизмов к антимикробным препаратам» и EUCAST
-
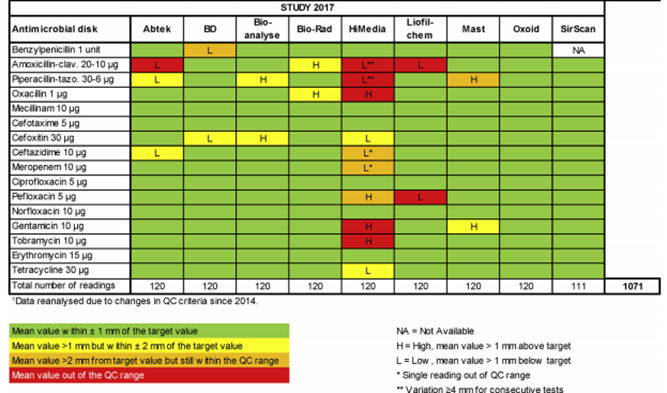
Диски с антибиотиками Bioanalyse (Турция). Показали хорошие результаты по результатам исследования EUCAST в 2017 году
Использованная литература:
Клинические рекомендации “Внутрилабораторный контроль качества питательных сред для клинических микробиологических исследований”, 2014.
МУК 4.2.2316-08 “Методы контроля бактериологических питательных сред: Методические указания”
Клинические рекомендации “Определение чувствительности микроорганизмов к антимикробным препаратам”, Версия 2015-2.
Приказ №535 Минздрава от 22 апреля 1985 года «Об унификации микробиологических методов исследования».
№ 125-ФЗ от 20.07.2012 «О донорстве крови и её компонентов». ст.17, п.2.
ВОЗ. Устойчивость к противомикробным препаратам
Нижегородцева И.А. Возможности современной микробиологической лаборатории. Опыт работы.
